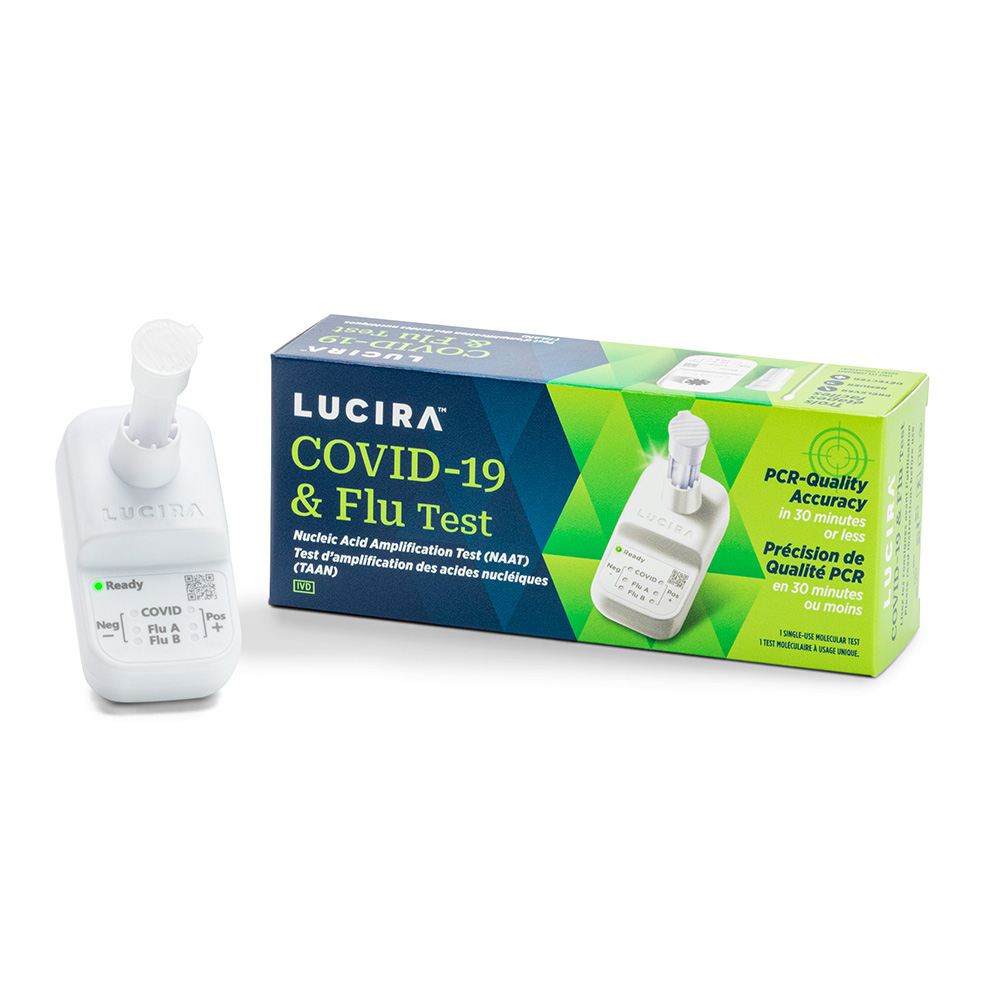
EMERYVILLE, Californie, 29 mars 2022 (GLOBE NEWSWIRE) — Lucira Health, Inc. (« Lucira Health » ou « Lucira ») (Nasdaq : LHDX), une entreprise de technologie médicale axée sur le développement et la commercialisation de tests de dépistage de maladies infectieuses transformateurs et novateurs, a annoncé que les résultats préliminaires des essais cliniques portant sur son test de dépistage candidat pour la COVID-19 et la grippe ont démontré une sensibilité et une spécificité similaires aux tests PCR ultra-sensibles en laboratoire pour la COVID-19, la grippe A et la grippe B.
« Ces données portant sur le test de dépistage de Lucira pour la COVID-19 et la grippe sont très importantes parce qu’elles démontrent que la possibilité de profiter de la sensibilité et de la spécificité des tests PCR en laboratoire dans la paume d’une main à la maison peut avoir des répercussions au-delà de la COVID-19 et s’appliquer à d’autres maladies infectieuses graves », a déclaré le Dr John Chou de Sutter Health et chercheur principal de l’étude.« Au fur et à mesure que la pandémie de COVID-19 évolue, notre raison principale de réaliser des tests de dépistage évolue aussi. Pour passer du test-visant-à-isoler au test-visant-à-traiter, nous aurons besoin d’outils diagnostiques rapides, précis et accessibles pour plusieurs maladies infectieuses. »
Bien que le test de dépistage de la COVID-19 soit devenu la norme pendant la pandémie, le test de dépistage de la grippe est rarement effectué et aucun test d’auto-dépistage à domicile pour la grippe n’était disponible, malgré des épidémies annuelles à grande échelle. Il est possible de traiter la COVID-19 et la grippe avec plusieurs antiviraux autorisés ou approuvés par la FDA qui sont considérés comme étant les plus efficaces lorsqu’ils sont pris tôt dans l’évolution de la maladie.
« À mesure que les gens délaissent le port du masque et ne respectent plus la distanciation sociale, il est plus probable que nous vivions le retour des épidémies de grippe avec la présence de la COVID-19 cet automne et cet hiver », a déclaré Debkishore Mitra, directeur de la technologie et cofondateur de Lucira Health. « Si vous souffrez d’une maladie pseudogrippale, il sera essentiel de connaître rapidement la nature de l’infection qui vous afflige afin que vous puissiez obtenir le traitement approprié et le commencer dès le début de la maladie. Nous sommes confiants que grâce à notre test de dépistage de la COVID-19 et de la grippe à domicile, des millions de personnes à travers le monde pourront profiter d’un diagnostic précis et d’un traitement adéquat. »
Des présentations réglementaires à la Food and Drug Administration des États-Unis, à Santé Canada, à l’Agence européenne des médicaments et à d’autres organismes de réglementation, sont prévues pour le deuxième trimestre de 2022 et des décisions sont attendues avant la prochaine saison de grippe.
À propos du test de dépistage de la COVID-19 et de la grippe de Lucira
Le test de Lucira pour le dépistage de la COVID-19 et de la grippe est un test moléculaire expérimental pour utilisation à domicile qui emploie la même plateforme et le même dispositif que les tests de Lucira pour le dépistage de la COVID-19 afin de fournir des diagnostics indépendants de la COVID-19, de la grippe A et de la grippe B. Le dispositif de ce test à usage unique tient dans la paume de votre main, fonctionne avec deux (2) piles AA, et avec un seul frottis nasal, il fournit un diagnostic positif ou négatif de la COVID-19, de la grippe A et de la grippe B en moins de 30 minutes.
À propos de l’étude clinique
Le test de Lucira pour le dépistage de la Covid-19 et de la grippe est présentement en évaluation chez plus de 600 sujets dans plusieurs centres d’études en Californie et au Texas, afin de comparer sa capacité à détecter avec précision la COVID-19, la grippe A et la grippe B à celle des tests de dépistage de la COVID-19 ultra-sensibles effectués en laboratoire sous autorisation d’urgence et à celle des tests PCR 510k approuvés pour la grippe. L’étude comprend des volets rétrospectifs et prospectifs au sein desquels les échantillons des sujets sont analysés à l’aide du dispositif Lucira et sont ensuite analysés avec un test de laboratoire PCR comparable.
À propos de Lucira Health
Lucira est une entreprise de technologie médicale axée sur le développement et la commercialisation de tests de dépistage de maladies infectieuses transformateurs et novateurs. La plateforme d’essai de Lucira produit des tests moléculaires de qualité de laboratoire dans une trousse de test à usage unique, conviviale, qui tient dans la paume de la main et qui est alimentée par deux piles AA. Lucira a conçu ses trousses de test de dépistage pour fournir des résultats d’analyse moléculaire sur place précis et fiables, et ce partout et en tout temps.
Au-delà de ses tests de dépistage de la COVID-19, Lucira travaille sur de nouveaux tests diagnostiques, y compris un test à usage unique pour la COVID-19 et l’influenza, ainsi que pour d’autres maladies infectieuses. Pour de plus amples renseignements, consultez le site www.lucirahealth.com.
Déclarations prospectives
Les déclarations contenues dans ce communiqué de presse concernant des questions qui ne sont pas des faits historiques sont des « déclarations prospectives » au sens de la Private Securities Litigation Reform Act de 1995. Puisque ces déclarations comportent des risques et des incertitudes, les résultats réels peuvent différer sensiblement de ceux exprimés ou sous-entendus par ces déclarations prospectives. Des mots tels que « peut », « prévoit », « sera », « pourrait », « anticipe », « s’attend à », « potentiel » et des expressions similaires, se reportent à des déclarations prospectives. Ces déclarations prospectives sont basées sur les attentes actuelles de Lucira et impliquent des présomptions qui pourraient ne jamais se concrétiser ou s’avérer incorrectes. Les résultats réels pourraient différer sensiblement de ceux anticipés dans de telles déclarations prospectives découlant de divers risques et incertitudes, y compris la capacité de Lucira d’augmenter la production, de rationaliser les opérations et d’augmenter la disponibilité du produit; le succès de la plateforme de test de dépistage de Lucira pour la COVID-19, y compris ses variants, la grippe A et la grippe B; l’ampleur et la durée de la pandémie de COVID-19 et les attentes de Lucira concernant la demande des consommateurs et des utilisateurs pour ses tests de dépistage et pour la trousse de dépistage candidate de la COVID-19 et de la grippe; la capacité de Lucira d’obtenir et de maintenir l’approbation réglementaire pour ses trousses de test de dépistage, y compris l’autorisation d’utilisation d’urgence existante de Lucira pour ses trousses de test de dépistage de la COVID-19 et LUCI Pass; les attentes de Lucira concernant le moment de la présentation et de la réception de l’approbation réglementaire pour ses trousses de test de dépistage; la performance des tierces parties, desquelles Lucira dépends, en lien avec la commercialisation de ses trousses de test de dépistage, y compris Jabil Inc, Switch Health et les fournisseurs exclusifs de Lucira; la capacité de Lucira de poursuivre son développement international; tout impact affectant la capacité de Lucira de commercialiser ses produits; demandes pour les produits de Lucira en raison de reports de procédures utilisant ses produits ou de perturbation de sa chaîne logistique; la capacité de Lucira d’atteindre ou de maintenir la rentabilité; la capacité de Lucira de s’assurer que ses produits soient acceptés sur le marché et de prévoir et de satisfaire adéquatement les demandes des clients; la capacité de Lucira de faire face à la concurrence avec succès; la capacité de Lucira d’améliorer et d’augmenter son offre de produits, y compris sa trousse de test de dépistage candidate de la COVID-19 et de la grippe; la capacité de Lucira de prédire son expansion continue; la capacité de Lucira de prévoir précisément ses revenus; problèmes de développement et de fabrication; les contraintes ou délais en matière de capacité de production des produits de Lucira; maintien de la couverture et remboursement adéquat pour les procédures utilisant les produits de Lucira; et défauts ou défaillances de produits. Ces risques et autres risques et incertitudes sont décrits plus en détail dans la section « Facteurs de risque » et ailleurs dans les documents déposés par Lucira auprès de la Securities and Exchange Commission et disponibles au www.sec.gov, y compris dans son plus récent rapport annuel sur le formulaire 10-K et son rapport trimestriel sur le formulaire 10-Q. Toute déclaration prospective faite par Lucira dans le cadre de cette annonce ne s’applique qu’à partir de la date du présent communiqué de presse, et Lucira n’a aucune obligation de mettre à jour les déclarations prospectives, que ce soit à la suite de nouveaux renseignements, d’événements à venir ou autrement après la date du présent communiqué de presse, sauf si la loi applicable l’exige.
Personne-ressource pour les médias
Mike Stommel
Lucira@luckybreakpr.com
323 333-2901

Lorem ipsum dolor sit amet consectetur adipiscing elit dolor

On April 21, 2022 Lucira Health and USA Boxing announce exclusive partnership for the 2022 season.
On March 30, 2022 Lucira Health announces that its PCR-Quality At-Home COVID-19 Test Now Available Direct to Consumers in Canada.
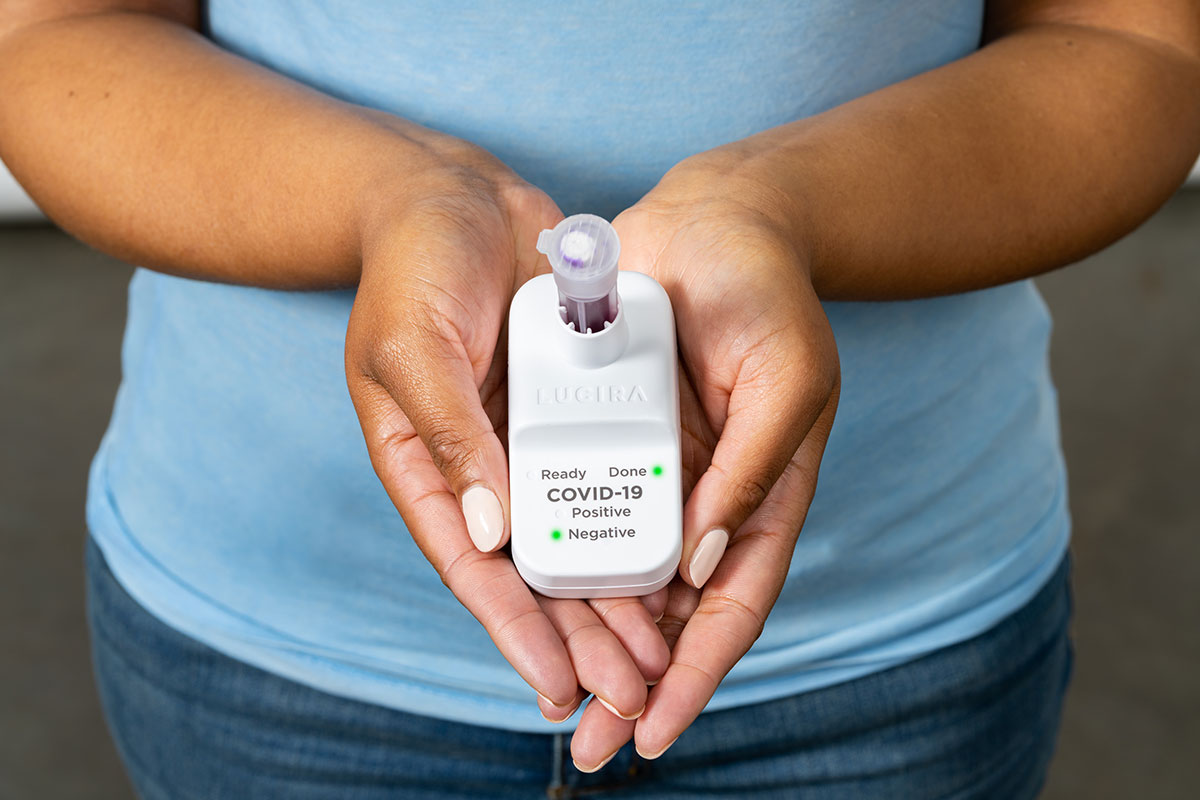
On March 30, 2022 Lucira Health announces that its PCR-Quality At-Home COVID-19 Test Now Available Direct to Consumers in Canada.
Ces autotests ont été autorisés par Santé Canada en vertu d'une autorisation d'arrêté provisoire. Le test Lucira COVID-19 & Grippe a été autorisé uniquement pour le test d'écouvillons nasaux d'individus symptomatiques pour la détection de l'acide nucléique du SRAS-CoV-2, de la grippe A et de la grippe B, et non pour d'autres virus ou agents pathogènes. Le test Lucira COVID-19 a été autorisé pour tester les prélèvements nasaux d'individus présentant ou non des symptômes pour la détection de l'acide nucléique du SRAS-CoV-2, et non pour d'autres virus ou agents pathogènes.
Pour demander plus d'informations nous contacter ou appelez le service client au 1-888-582-4724
Monday -Friday 7:00am-5:00pm PT
Pour les demandes générales des médias, veuillez contacter Lucira@luckybreakpr.com. If your media request is urgent, please contact: media@lucirahealth.com
© 2023 Lucira Health, Inc. All rights reserved.